 |
|
|
![]()
![]() Определение
жесткости воды
Определение
жесткости воды
![]() химическое обессоливание с помощью ионитов
химическое обессоливание с помощью ионитов
![]() смешивание с более мягкой водой
смешивание с более мягкой водой
![]()
Определение жесткости воды
Жесткость воды измеряют методом титрования веществом сложного химического состава, называемым двунатриевой солью этилендиаминтетрауксусной кислоты, или условно трилоном Б.
Это вещество образует с ионами кальция и магнии, характеризующими жесткость воды, растворимые внутрикомплексные соединения. Если в воду, содержащую ионы кальция и магния, ввести раствор индикатора (красителя), меняющего цвет в их присутствии, а затем добавить туда трилон Б, то в эквивалентной точке произойдет изменение ем окраски. В качестве индикатора обычно применяют эрихром черный Т или хромовый темно-синий.
Методика точного определения жесткости воды состоит в следующем.
-
Готовят сантинормальный (0,01 н) раствор трилона Б. В 700 мл дважды дистиллированной воды (или химически обессоленной) растворяют 1,86 г трилона и объем раствора доводят до 1 л. Приготовляют буферный раствор, служащий для поддержания рН испытуемого раствора в пределах выше 9 (индикаторы изменяют свой цвет не только в присутствии ионов кальция и магния, но и при изменении рН), для чего растворяют 20 г хлористого аммония в дистиллированной воде, добавляют 100 мл 25%-ного раствора аммиака и доводят до 1 л дистиллированной воды.
Готовят раствор индикатора. Разводят хромовый темно-синий в количестве 0,5 г в 20 мл буферного раствора и доводят до 100 мл этиловым спиртом. Если вместо хромового темно-синего берут эрихром черный Т, то нужно учитывать, что раствор его менее стоек и его можно готовить не более чем на 10 суток.
Определяют жесткость воды. Для этого берут исследуемую воду в объеме 10 мл, добавляют 1 мл буферного раствора и 1 - 2 капли раствора индикатора. При этом раствор окрашивается в розово-красный цвет. Далее из микробюретки по каплям и при постоянном помешивании вводят раствор трилона Б до изменения окраски из розовой в синюю. В момент окрашивания раствора в синий цвет замечают количество израсходованного на это хрилона Б (в мл). Это количество и будет равно жесткости воды (в мг-экв/л), принятой по ГОСТу. Однако в аквариумной практике жесткость воды считают не в мг-экв/л, а в градусах жесткости наших или немецких, которые численно равны между собой (один немецкий градус равен 0,36 мг-экв/л, следовательно, 1 мг-экв/л равен 2,804 градуса, или 2,8°).
Если при приготовлении трилона Б взять навеску его не 1,86, а в 2,3 раза меньше (0,66 г), то жесткость воды будет измеряться непосредственно в градусах, то есть 1 мл пошедшего на титрование трилона Б будет равен 1° жесткости воды.
Раствор трилона Б, приготовленный для титрования, требует уточнения титра. Вызвано это тем, что трилон Б, как это было сказано выше, сложное химическое соединение, и даже точная его навеска требует химической проверки. Делают это следующим образом: готовят 0,01 н раствор фиксанала сернокислого магния (фиксанал - особо чистое вещество точной навески). Для этого ампулу фиксанала всыпают в 700 - 800 мл дважды дистиллированной воды, растворяют соль и этим же раствором, а затем дистиллированной водой ополаскивают ампулу, чтобы смыть остатки соли. Затем в мерной колбе раствор доводят до 1 л. Применение во всех случаях приготовления растворов мерной колбы необходимо, так как обеспечивает более точный отмер жидкости, чем мерные цилиндры и стаканы. Растворы сернокислого магния сохраняются долго. Установку титра производят так: к 10 мл 0,01 н раствора сернокислого магнит (фиксанала) прибавляют 1 мл буферного раствора, 1 - 2 капли индикатора и титруют трилоном Б, как при определении жесткости.
Определяют коэффициент титра по формуле:
![]()
К - коэффициент титра, а - расход трилона Б. Она пригодна для сантинормального раствора трилона и определения жесткости воды в мг-экв/л. Если раствор трилона приготовлен для определения жесткости в градусах, то применяется формула поправочного коэффициента:
![]()
В дальнейшем при измерениях: полученный коэффициент нужно умножать, на результат измерений. Пользуясь этим методом, можно скорректировать раствор трилона так, чтобы коэффициент стал равным единице (К = 1).
Учитывая, что высокая точность определения жесткости воды нужна не во всех случаях аквариумной практики, можно упростить изложенную ранее методику измерений. Она будет пригодна для определения жесткости воды с точностью 0,5°.
Условно 1 капля жидкости из обычной пипетки имеет объем 0,04 мл (так считают медики и химики), тогда, несколько изменив концентрацию, буферный раствор готовят следующим образом: 2,7 г хлористого аммония растворяют в 18 мл 25%-ного аммиака и разбавляют дистиллированной водой до 50 мл. Далее в полученный раствор добавляют 0,25 г хромогена синего, растирают его и доводят до 100 мл спиртом.
В полученном составе растворяют 0,83 г трилона Б и таким образом получают комбинированный раствор для определения жесткости воды, 1 капля которого эквивалентна 0,5° жесткости.
Результат работы проверяют по фиксаналу сернокислого магния и, если потребуется, корректируют. На титрование 10 мл фиксанала, должно пойти 56 капель комбинированного раствора.
Для определения жесткости воды в домашних условиях обзаводятся следующим оборудованием: мензуркой на 100 мл, микробюреткой на 2 - 5 мл и мерной пипеткой на 5 мл. Реактивами служат раствор трилона Б концентрацией 0,1 нормального раствора, аммиачный буферный раствор и раствор эриохрома черного Т. Ход анализа таков. В колбу к 100 мл исследуемой воды сначала добавляют 5 мл аммиачного раствора, а затем 5 - 10 капель раствора индикатора. Вода становится бледно-розовой или темно-вишневой (чем выше жесткость, тем интенсивнее окраска). После этого титруют смесь трилоном Б, взбалтывая раствор после каждой капли. Появление сине-зеленоватого цвета — сигнал к окончанию титрования. Дальнейший пересчет ведут по формуле:
X = Q A 1000/B,
где Х — жесткость воды в немецких градусах; Q — количество затраченного трилона Б, мл; А — концентрация раствора трилона Б; В — объем исследованной воды, мл.
Табл. 4 поможет рассчитать жесткость воды.
Таблица 4
|
Жесткость воды, dGH |
0 |
0,1 |
0,2 |
0,3 |
0,4 |
0,5 |
0,6 |
0,7 |
0,8 |
0,9 |
|
0 |
- |
0,036 |
0,071 |
0,10 |
0,14 |
0,18 |
0,21 |
0,25 |
0,28 |
0,32 |
|
1 |
0,36 |
0,39 |
0,43 |
0,46 |
0,50 |
0,53 |
0,57 |
0,60 |
0,64 |
0,68 |
|
2 |
0,71 |
0,75 |
0,78 |
0,82 |
0,85 |
0,89 |
0,93 |
0,96 |
1,00 |
1,03 |
|
3 |
1,07 |
1,10 |
1,14 |
1,18 |
1,21 |
1,25 |
1,28 |
1,32 |
1,35 |
1,39 |
|
4 |
1,43 |
1,46 |
1,50 |
1,53 |
1,57 |
1,60 |
1,64 |
1,68 |
1,71 |
1,75 |
|
5 |
1,78 |
1,82 |
1,85 |
1,89 |
1,92 |
1,96 |
2,00 |
2,03 |
2,07 |
2,10 |
|
6 |
2,14 |
2,17 |
2,21 |
2,25 |
2,28 |
2,32 |
2,35 |
2,39 |
2,42 |
2,46 |
|
7 |
2,50 |
2,53 |
2,57 |
2,60 |
2,64 |
2,67 |
2,71 |
2,75 |
2,78 |
2,82 |
|
8 |
2,85 |
2,89 |
2,92 |
2,96 |
2,99 |
3,03 |
3,07 |
3,10 |
3,14 |
3,17 |
|
9 |
3,20 |
3,24 |
3,28 |
3,32 |
3,35 |
3,39 |
3,42 |
3,46 |
3,50 |
3,53 |
|
10 |
3,57 |
3,60 |
3,64 |
3,67 |
3,71 |
3,74 |
3,78 |
3,81 |
3,85 |
3,89 |
|
11 |
3,92 |
3,96 |
3,99 |
4,03 |
4,06 |
4,10 |
4,14 |
4,17 |
4,21 |
4,24 |
|
12 |
4,28 |
4,31 |
4,35 |
4,39 |
4,42 |
4,46 |
4,49 |
4,53 |
4,56 |
4,60 |
|
13 |
4,63 |
4,67 |
4,70 |
4,74 |
4,79 |
4,81 |
4,85 |
4,88 |
4,92 |
4,96 |
|
14 |
4,99 |
5,03 |
5,06 |
5,10 |
5,13 |
5,17 |
5,21 |
5,24 |
5,28 |
5,31 |
|
15 |
5,35 |
5,38 |
5,42 |
5,45 |
5,49 |
5,53 |
5,56 |
5,60 |
5,63 |
5,67 |
Пример расчета. Анализ проводили трилоном Б - 0,1 н в 100 мл воды, расход составил 2,96. В таблице отыскиваем цифру 2,96. В боковике против этой цифры находятся целые градусы, т. е. 8, в верхней графе — десятые доли (т. е. 0,3). Таким образом, жесткость в нашем случае будет равна 8,3°. Приведенной таблицей можно пользоваться при трилоне Б - 0,01 н и 100 мл (при этом конечный расход трилона уменьшают в 10 раз), а также при трилоне Б - 0,05 н и 50 мл.
Косвенно о степени жесткости воды судят по ее мылкости: мягкая вода при сбивании мгновенно образует обильную пену, очень жесткая практически не пенится. Справку о жесткости питьевой воды можно получить на водопроводной станции или в районной инспекции санитарно-ветеринарного надзора.
Теперь мы научились измерять общую жесткость воды. Но аквариумисту иногда нужно знать показатель не только общей жесткости, но и так называемой временной, или карбонатной, частично устраняемой кипячением. Для измерении его готовят комбинированный раствор: 0,03 г метилоранжа (индикатор) растворяют в 25 мл дважды дистиллированной воды, затем добавляют 0,7 мл соляной кислоты марки Х. Ч. или Ч. Д. А и доводят объем до 100 мл дважды дистиллированной водой. Раствор имеет красный цвет. При добавлении капли его к воде, имеющей карбонатную жидкость, она окрашивается в желтый цвет. Добавляя раствор в воду по каплям (при постоянном помешивании) до получения оранжевой окраски и считая капли, измеряют карбонатную жесткость. Одна капля раствора эквивалентна 0,5°.
К физическим методам уменьшения жесткости относят дистилляцию и электролиз, к химическим — ионообмен (с помощью сильных и слабых катионитов и анионитов), обработку известью, щавелевой и фосфорной кислотами, а также диффузионный метод. Простейшими способами умягчения воды являются кипячение (15 - 20 мин) и вымораживание (жесткость падает с 15 до 3°).
Для смягчения водопроводной воды ее разбавляют в нужной пропорции дистиллированной или химически обессоленной, измеряя при этом полученный результат или пользуясь данными, приведенными в таблице 5.
Таблица 5
Количество дистиллированной воды,
которое нужно добавить к 1 л водопроводной, чтобы получить воду нужной жесткости
|
Нужная жесткость воды |
Исходная жесткость воды |
|||||||||
|
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
|
3 |
1000 |
1333 |
1666 |
2000 |
2333 |
2666 |
3000 |
3333 |
3666 |
4000 |
|
4 |
500 |
750 |
1000 |
1250 |
1500 |
1750 |
2000 |
2250 |
2500 |
2750 |
|
5 |
200 |
400 |
600 |
800 |
1000 |
1200 |
1400 |
1600 |
1800 |
2000 |
|
6 |
- |
166 |
333 |
500 |
666 |
833 |
1000 |
1168 |
1333 |
1500 |
|
7 |
- |
- |
142 |
285 |
428 |
571 |
714 |
857 |
1000 |
1143 |
|
8 |
- |
- |
- |
125 |
150 |
375 |
500 |
625 |
750 |
875 |
|
9 |
- |
- |
- |
- |
111 |
222 |
333 |
444 |
556 |
667 |
|
10 |
- |
- |
- |
- |
- |
100 |
200 |
300 |
400 |
500 |
|
11 |
- |
- |
- |
- |
- |
- |
91 |
182 |
273 |
364 |
|
12 |
- |
- |
- |
- |
- |
- |
- |
83 |
167 |
250 |
Вот несколько способов понижения жесткости воды:
На дно сосуда из жаропрочного материала кладут кусочки фарфора, обеспечивающие равномерное кипение, наливают воду, закрывают пробкой с отверстием, в которое вставляют конец стеклянной трубки или змеевика, связанный с холодильником (рис.3). При кипячении воды ее пары конденсируются в холодильнике, и дистиллированная вода стекает в сосуд. Жесткость получаемой воды — dH 0,8 - 2,3°. При необходимости можно провести повторную дистилляцию и получить воду жесткостью 0,2 - 0,8°. Недостаток процесса — малая производительность;
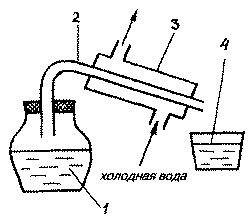
Рис. 3. Схема
дистилитора:
1 -колба с водой, 2 - стеклянная трубка, 3 - холодильник,
4 - сосуд для дистиллированной воды.
химическое обессоливание с помощью ионитов:
В аквариумной практике рекомендуют использовать катиониты КУ-2, КУ-23 и аниониты АВ-17. Катионит обменивает все катионы, содержащиеся в воде, на катион Н+, а анионит — все анионы на ион ОН-, которые, соединившись, дают полностью обессоленную воду.
Прибор состоит из стеклянных цилиндров диаметром 40 - 60 мм и длиной 400 - 600 мм, укрепленных на штативе, соединенных трубками между собой, с водопроводным краном и с сосудом для приема обессоленной воды. Цилиндры со слоем стекловаты на дне закрыты резиновыми пробками с отверстием в центре, в которое вставлена стеклянная трубка с надетой на нее резиновой (рис. 4).
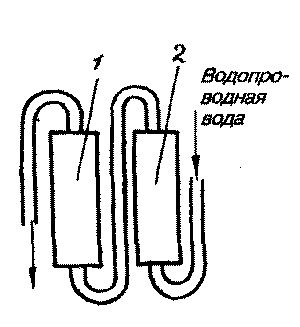 Рис.
4. Схема ионообменника:
Рис.
4. Схема ионообменника:
1 - цилиндр с анианитом,
2 - цилиндр с катионитом.
Иониты разбухают в воде, и для того, чтобы они не разорвали цилиндры, их в отдельном сосуде заливают водой и отстаивают 10 - 12 ч. Затем катионит засыпают в цилиндр, пропускают через него 5% раствор соляной кислоты в дистиллированной воде из расчета 400 мл раствора на 100 г сухого катионита и промывают дистиллированной водой объемом в 2 раза большим, чем объем израсходованной кислоты. В другой цилиндр засыпают анионит, через него пропускают 5% раствор гидроксида натрия в дистиллированной воде из расчета 300 мл раствора на 100 г сухого анионита и промывают дистиллированной водой объемом в 3 раза больше, чем объем израсходованной щелочи. Затем прибор собирают и пропускают через него водопроводную воду. Жесткость полученной воды - 0,2 - 0,4°. Когда жесткость начнет повышаться, необходимо провести регенерацию ионитов, для чего отключить цилиндры и обработать ионит в одном случае кислотой, в другом — щелочью, как указано выше. В нерабочем состоянии цилиндры должны быть залиты дистиллированной водой, иониты, же долгое время стоявшие без применения, нуждаются в регенерации;
Воду наливают в низкий (200 - 300 мм) и возможно большего диаметра эмалированный или морозостойкий пластмассовый сосуд и ставят на мороз или в морозильник. После того как вода наполовину высоты сосуда замерзнет, пробивают лед, воду выливают, а лед растапливают. Полученная изо льда вода обычно имеет жесткость (в зависимости от начальной) 1 - 3°;
смешивание с более мягкой водой:
Перед смешиванием водопроводную воду подогревают 40 мин при 90° С, а затем охлаждают на воздухе.
Ниже приведены формулы, по которым в зависимости от жесткости, можно определить необходимый объем воды:
Vм =Vп х (dHв - dHп) : (dHa - dHм);
Vв = Vп х (dHп - dHм) : (dHa - dHм);
Vп = Vм x (dHa - dHм) : (dHa - dHп),
где V - объем воды; индексы: в - водопроводная вода, м - мягкая вода, п - получаемая вода;
Воду кипятят в течение 1 ч в эмалированной посуде, охлаждают и сливают 2/3 верхнего слоя, у которого жесткость будет снижена за счет понижения временной жесткости. При этом способе вода теряет ряд питательных веществ, необходимых растениям;
применение дождевой или снеговой воды:
 Которые
имеют жесткость dH; до 3°, можно рекомендовать лишь в районах, где атмосфера
не загрязнена промышленностью. Во всяком случае, ее нужно отстаивать несколько
недель, а затем, взяв верхний слой, фильтровать через активированный уголь
и несколько дней аэрировать, после чего, смешав в нужной пропорции с обычной
водой для получения необходимой жесткости и рН, проверить пригодность
на дешевых рыбах;
Которые
имеют жесткость dH; до 3°, можно рекомендовать лишь в районах, где атмосфера
не загрязнена промышленностью. Во всяком случае, ее нужно отстаивать несколько
недель, а затем, взяв верхний слой, фильтровать через активированный уголь
и несколько дней аэрировать, после чего, смешав в нужной пропорции с обычной
водой для получения необходимой жесткости и рН, проверить пригодность
на дешевых рыбах;
Катасонов для приготовления мягкой воды предложил использовать устройство, предложенное Кротовым для получения “мертвой” и “живой” воды (рис.5). Используемая им конструкция состоит из эмалированного бидона емкостью 3 л, в который помещен стакан высотой 185 мм и 0 65 мм, сшитый из плотного брезента капроновыми нитками, и двух электродов из нержавеющей стали размером 190 х 30 мм и толщиной 1,5 - 2 мм, получающих питание от сети переменного тока 220 В через диодный мост. Такое устройство через 10 мин работы позволяет получить 2,5л воды с dH около 0° и рН 4,2, которая имеет желтовато-лимонный цвет, кисловатый запах и находится в самом бидоне (“мертвая” вода). Воду сливают в сосуд, дают остыть и затем подщелачивают питьевой содой до нужного значения рН, после чего отстаивают несколько дней, в течение которых на дне скопится осадок желтовато-коричневого цвета.
Повышение жесткости воды до 10° благоприятно сказывается на большинстве даже мягководных видов. Непреложным правилом считается постепенное увеличение минерализации воды сразу после выклева эмбрионов у выходцев из Амазонки, Конго, Нигера, Амура и т. д. Жесткая вода совершенно необходима малавийским и танганьикским рыбам, живородящим, тетраодонам, атеринам и т. д. Добавление 1 мл 10%-ного раствора хлористого кальция, продающегося в аптеке, увеличивает жесткость литра воды примерно на 2,9°, а 1 мл 25%-ного раствора сульфата магния — на 4°. С этой целью нельзя применять толченый известняк, так как он нарушает катионный баланс воды.
Для получения воды требуемой жесткости используют следующие формулы:
![]()
где х, у и z — соответственно количество жесткой, мягкой и полученной воды, л; а, b и с — соответственно жесткости жесткой, мягкой и полученной воды, немецкие градусы.
Примеры.
1. Из водопроводной воды жесткостью 10° и мягкой 0,3° нужно получить 10 л воды жесткостью 1,5%. Произведя расчеты, получим:
![]()
Следовательно, надо взять 1,24 л мягкой и 8,76 л жесткой воды. При ограниченном количестве мягкой воды рассчитывают, какое количество воды необходимой жесткости можно получить, смешав ее с водопроводной.
2. Есть 5 л мягкой воды жесткостью 0,1° и водопроводной воды 12°. Нужно получить воду жесткостью 3°:
![]()
Итак, к имеющейся мягкой воде надо добавить 6,61 л водопроводной.
Если нужно увеличить жесткость воды, лучше воспользоваться так называемой гипсовой водой. Для ее приготовления 2 г гипса (можно технического) размешивают в 1 л воды, дают отстояться в течение 2 - 3 суток, временами перемешивая раствор.
После отстоя гипсовую воду сливают и добавляют к мягкой воде. Жесткость полученной гипсовой воды лежит в пределах 75°.


